Кристаллические решетки. Разделы: Химия, Конкурс «Презентация к уроку»Презентация к уроку. Загрузить презентацию (3,4 МБ). Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации.
Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию. Тип урока: Комбинированный. Основная цель урока: Дать учащимся. Задачи урока. Образовательная: сформировать понятия о. Воспитательная: продолжить формирование.
Вещества молекулярного и немолекулярного строения. Простые и сложные вещества. Для этого рассмотрим таблицу 1. СЛО́ЖНОЕ ВЕЩЕСТВО́, вещество, молекула которого состоит из атомов 2 или более различных химических элементов. . Презентация "Атомно-молекулярное учение" Разработка урока химии в 8. Ионы. Вещества немолекулярного строения. Цели урока. Вещества молекулярного и немолекулярного строения Цели урока: Обобщить и углубить знания учащихся о зависимости. - презентация. Презентация была опубликована 2 года назад пользователемКлавдия Мельникова..
Развивающая: развивать познавательный. Оборудование: Периодическая система. Д. И. Менделеева, коллекция “Металлы”, неметаллы. Презентация “Кристаллические решетки”, модели. Возгонка. бензойной кислоты”. Ход урока. 1. Организационный момент.
Учитель приветствует учеников, фиксирует. Затем сообщает тему урока и цель урока.
Учащиеся записывают тему урока в тетрадь. Cлайд 1. 2). 2. Проверка домашнего задания(2 ученика у доски: Определить вид химической. Na. Cl, CO2, I2 ; 2) Na, Na. OH, H2. S. (записывают ответ на доске и включаются в опрос). Анализ ситуации. Учитель: Что изучает химия? Ответ: Химия - это. Учитель: Что же такое вещество?
Ответ. Вещество - это то, из чего состоит физическое. Cлайд 3). Учитель: Какие агрегатные состояния веществ. Ответ: Существует три агрегатных. Cлайд. 4). Учитель: Приведите примеры веществ, которые.
Вещества молекулярного и немолекулярного строения. Зависимость свойств веществ от особенностей их кристаллической решетки. Ранее мы познакомились со следующими видами химической связи: ионная, металлическая, ковалентная полярная и неполярная..
Ответ: Вода. При обычных условиях вода. С вода переходит в. С мы получим водяной пар. Учитель (дополнение): Любое вещество можно.
Кроме воды – это металлы, которые при нормальных. При дальнейшем. нагревании, до температуры кипения, металлы.
Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Под строением вещества понимают, из каких частиц (молекул, ионов, атомов) построена его кристаллическая решетка..
Любой газ можно. перевести в жидкое и твердое состояние, понижая. С) превращается в жидкость. С). затвердевает в снегообразную массу, состоящую из. Сегодня на уроке мы. Учитель: Назовите, какие твердые вещества.

Ответ: Металлы, пластилин, поваренная соль. Na. Cl, графит. Учитель: Как вы думаете? Какое из этих веществ. Ответ: Пластилин. Учитель: Почему? Делаются предположения. Если ученики. затрудняются, то с помощью учителя приходят к.
Таков, например, шоколад, который тает во рту, или. Такие вещества называют аморфными.
Cлайд. 6). Таким образом, различают два вида твердых. У аморфных веществ нет определенной. Кристаллические вещества имеют строго.
Эти частицы расположены в строго. Cлайд 8)Учитель задаетпроблемные вопросы. Как объяснить существование твердых веществ со. Почему кристаллические вещества при ударе. Выслушать ответы учеников и подвести их к выводу: Свойства веществ в твердом состоянии зависят. Cлайд 9). Проверка домашнего задания: 1) Na.
Cl – ионная связь, СО2 – ковалентная полярная связь I2 – ковалентная неполярная связь 2) Na – металлическая связь. Nа. ОН - ионная связь между Na+и.
ОН- (О и Н. ковалентная)Н2. S - ковалентная полярная. Фронтальный опрос.
Какая связь называется ионной? Какая связь называется ковалентной? Какая связь называется ковалентной полярной?
Что называется электроотрицательностью? Вывод: Прослеживается логическая. Строение атома—> ЭО—> Виды химической. Тип кристаллической. Свойства веществ. Учитель: В зависимости от вида частиц и от. Cлайд. 1. 1). Далее идет рассмотрение типов кристаллических.
Особое внимание уделяется взаимосвязи. Результаты оформляются в следующую. Приложение 1). (Cлайд 1. Ионные кристаллические решетки(Cлайд. Учитель: Как вы думаете?
Для веществ с каким. Ответ: Для веществ с ионной химической.
Учитель: Какие частицы будут находиться в. Ответ: Ионы. Учитель: Какие частицы называются ионами? Ответ: Ионы- это частицы, имеющие. Учитель: Какие ионы бывают по составу? Ответ: Простые и сложные.
Демонстрация - модель кристаллической решетки. Na. Cl). Объяснение учителя: В узлах кристаллической. В кристаллах Na. Cl отдельных молекул хлорида. Весь кристалл следует. Na+ и Cl- . Nan. Cln, где n – большое число.
Связи между ионами в таком кристалле очень. Поэтому вещества с ионной решеткой. Они. тугоплавки, нелетучи, хрупки.
Расплавы их. проводят электрический ток (Почему?), легко. Ионные соединения - это бинарные соединения. I А и II A), соли, щелочи. Атомные кристаллические решетки(Слайд 1. Демонстрация кристаллических решеток алмаза и. У учеников на столе образцы графита.
Учитель: Какие частицы будут находиться в. Ответ: В узлах атомной кристаллической. Учитель: Какая химическая связь между. Ответ: Ковалентная химическая связь.
Объяснения учителя. Действительно, в узлах атомных кристаллических. Так как атомы. подобно ионам, могут по- разному располагаться в. Атомная кристаллическая решетка. В данных решетках молекулы отсутствуют.
Весь. кристалл следует рассматривать как гигантскую. Примером веществ с таким типом. Вопрос: Какие эти вещества по составу? Ответ. Простые по составу. Атомные кристаллические решетки имеют не.
Например, оксид. алюминия, оксид кремния. Все эти вещества имеют. С), прочны и тверды, нелетучи.
Металлические кристаллические. Слайд. 15)Учитель: Ребята, у вас на столах коллекция. Вопрос: Какая химическая связь характерна. Ответ: Металлическая.
Связь в металлах. Вопрос: Какие общие физические свойства.
Ответ: Блеск, электропроводность. Вопрос: Объясните, в чем причина того, что у. Ответ: Металлы имеют единое строение. Демонстрация моделей кристаллических решеток. Объяснение учителя.
Вещества с металлической связью имеют. В узлах таких решеток находятся атомы и.
Электроны электростатически. Этим. объясняется стабильность решетки. Молекулярные кристаллические решетки(Слайд. Учитель демонстрирует и называет вещества: йод. Вопрос: Что объединяет эти вещества? Ответ: Эти вещества являются неметаллами.
Простые по составу. Вопрос: Какая химическая связь внутри. Ответ: Химическая связь внутри молекул. Вопрос: Какие физические свойства для них. Ответ: Летучие, легкоплавкие. Учитель: Давайте сравним свойства металлов и. Ученики отвечают, что свойства.
Вопрос: Почему свойства неметаллов сильно. Ответ: У металлов связь металлическая, а у. Учитель: Следовательно, и тип решетки другой. Молекулярная. Вопрос: Какие частицы находятся в узлах. Ответ: Молекулы. Демонстрация кристаллических решеток.
Объяснение учителя. Молекулярная кристаллическая. Как видим, молекулярную кристаллическую.
H2,O2,N2, I2. O3, белый фосфор Р4, но и сложные. Большинство твердых органических. В узлах решеток находятся неполярные или. Несмотря на то, что атомы. Вывод: Вещества непрочные, имеют малую. Вопрос: Какой процесс называется. Ответ: Переход вещества из.
Демонстрация опыта: возгонка бензойной кислоты. Работа с заполненной таблицей.
Приложение 1. (Слайд 1. Кристаллические решетки, вид связи и. Тип решетки. Виды частиц в узлах. Вид связи между частицами.
Примеры веществ. Физические свойства веществ. Ионная. Ионы. Ионная – связь прочная. Соли, галогениды (IA,IIA),оксиды и. Твердые, прочные, нелетучие. Атомная. Атомы. 1.
Ковалентная неполярная - связь. Ковалентная полярная - связь. Простые вещества. C), графит(C) , бор(B), кремний(Si).
Сложные. вещества: оксид алюминия (Al. O3), оксид. кремния (IY)- Si. O2. Очень твердые, очень.
Молекулярная. Молекулы. Между молекуми- слабые силы. Твердые вещества при особых. О2,Н2,Cl. 2,N2,Br.
H2. O, CO2,HCl); сера, белый фосфор, йод; органические вещества. Непрочные, летучие. Металлическая. Атом- ионы. Металлическаяразной прочности. Металлы и сплавы. Ковкие, обладают блеском.
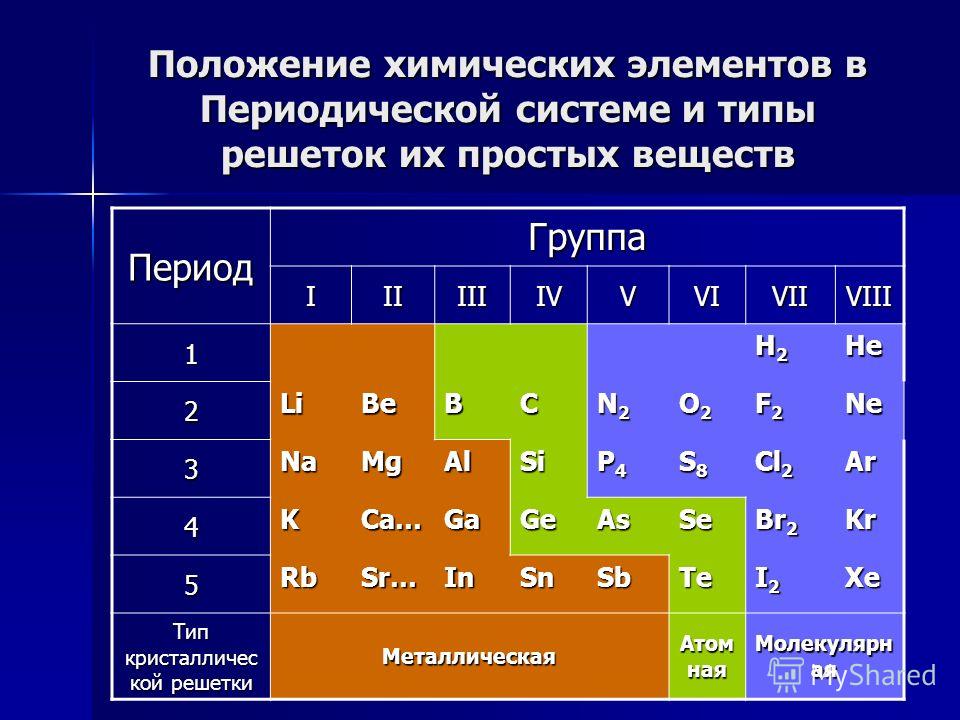
Вопрос: Какой тип кристаллической решетки. Ответ: Ионные кристаллические решетки. Вопрос: Какие кристаллические решетки. Ответ: Для простых веществ- металлов- . Работа с Периодической системой Д.
И. Менделеева. Вопрос: Где в Периодической системе. Элементы- неметаллы и почему? Ответ: Если провести диагональ от бора до. Это элементы I A, II A, III A. Элементы- неметаллы находятся в верхнем правом. Это элементы IY A,Y A, YI A, YII A, YIII A.
Учитель: Давайте найдем элементы неметаллы, у. Ответ: С, В, Si) и. Ответ: N, S, O, галогены и. Учитель: Сформулируйте вывод, как можно. Периодической системе Д. И. Менделеева. Ответ: Для элементов- металлов, которые.
I A, II A, IIIA (кроме бора), а также олова и. Для элементов- неметаллов IY A и бора в простом.
Y A, YI A, YII A, YIII A в простых веществах. Продолжаем работать с заполненной таблицей. Учитель: Посмотрите внимательно на таблицу. Какая закономерность прослеживается?
Внимательно слушаем ответы учеников, после. Существует следующая закономерность: если. Cлайд. 1. 8). Учитель: Посмотрите внимательно на таблицу.
Какую еще классификацию веществ вы можете. Если ученики затрудняются, то учитель. Cлайд 1. 9). Вещества молекулярного строения состоят из.
Вещества немолекулярного строения состоят из. Закон постоянства состава(Слайд 2. Учитель: Сегодня мы познакомимся с одним из. Это закон постоянства. Ж. Л. Прустом. Закон справедлив только для веществ. В настоящее время закон. Молекулярные химические.
Но для. веществ с немолекулярным строением этот закон не. Теоретическое и практическое значение закона. Вывод: химическая формула вещества. Cлайд 2. 1)Например, SO3: 1. Конкретное вещество - серный газ, или оксид.
YI). 2. Тип вещества - сложное; класс - оксид. Качественный состав - состоит из двух. Количественный состав - молекула состоит из. Относительная молекулярная масса - Mr(SO3)=. Молярная масса - М(SO3) = 8. Много другой информации.
Закрепление и применение полученных знаний(Слайд 2. Игра в крестики- нолики: зачеркните по. Na. Cl. N2. OMg(OH)2. CO2. K2. SNH3. Cl. O2. Na. OH Мg. Cl. H2. ONa. Na. NO3. SO2. KOHKCl. 2HCl.
Рефлексия. Учитель задает вопрос: “Ребята, что нового вы. Подведение итогов занятия. Учитель: Ребята, давайте подведем основные. Какие классификации веществ вы узнали? Как вы понимаете термин кристаллическая.
Какие типы кристаллических решеток вы теперь. О какой закономерности строения и свойств.
В каком агрегатном состоянии вещества имеют. С каким основным законом химии вы. Cлайд 2. 4)Домашнее задание: §2. Составьте формулы веществ: хлорид кальция. IY), азот, сероводород. Определите тип кристаллической решетки и.
Творческое задание —> составить вопросы к. Учитель благодарит за урок. Выставляет отметки.
 RSS Feed
RSS Feed
